Covid-19 : l'EMA met fin à l'examen du médicament développé par Eli Lilly
L'Agence européenne des médicaments a mis fin à l'examen d'une possible autorisation de mise sur le marché de l'Union européenne d'un médicament contre le Covid-19, après que son producteur, la firme pharmaceutique américaine Eli Lilly, s'est retiré du processus, invoquant une demande trop faible des États membres.
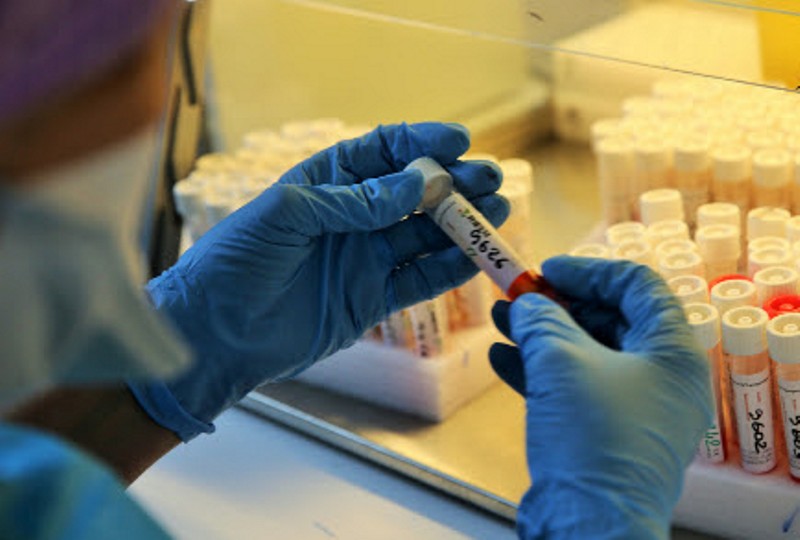
Covid-19 : l'EMA met fin à l'examen du médicament développé par Eli Lilly
Partager :
-
Pour ajouter l'article à vos favorisS'inscrire gratuitement
identifiez-vousVous possédez déjà un compte ?
Se connecterL'article a été ajouté à vos favoris -
Pour accéder à vos favorisS'inscrire gratuitement
identifiez-vousVous possédez déjà un compte ?
Se connecter
Le 3 novembre 2021 à 14h15
Modifié 3 novembre 2021 à 16h00L'Agence européenne des médicaments a mis fin à l'examen d'une possible autorisation de mise sur le marché de l'Union européenne d'un médicament contre le Covid-19, après que son producteur, la firme pharmaceutique américaine Eli Lilly, s'est retiré du processus, invoquant une demande trop faible des États membres.
"Compte tenu de la demande actuelle des États membres de l'Union européenne, Eli Lilly prévoit qu'aucune nouvelle campagne de fabrication de substances médicamenteuses ne sera nécessaire dans un avenir prévisible", souligne Eli Lilly, dans un courrier adressé à l'Agence européenne des médicaments (EMA).
Rappelant que son Comité des médicaments à usage humain (CHMP) a entamé la procédure liée à ce médicament en mars 2021, l'Agence européenne des médicaments précise que la firme pharmaceutique américaine se réserve le droit de demander un autre examen, ou de soumettre une demande d'autorisation de mise sur le marché à l'avenir.
Le traitement en question associe les anticorps Bamlanivimab et Etesevimab pour le traitement des patients Covid qui n'ont pas besoin d'oxygène, mais qui sont à risque de développer une forme grave de la maladie. Les anticorps monoclonaux, fabriqués en laboratoire, doivent désactiver le virus après une contamination.
L'EMA avait rendu en mars un avis positif sur l'usage de ces anticorps chez les patients Covid. Le retrait d'Eli Lilly du processus d'autorisation européenne n'y change rien : les patients peuvent continuer à recevoir les anticorps, en fonction des dispositions nationales, précise l'EMA.
La Commission européenne avait conclu, il y a quelques semaines, un accord-cadre relatif à l'achat conjoint du médicament d'Eli Lilly au niveau de l'Union européenne. Dix-huit États membres de l'UE y avaient pris part, pour 220.000 doses du traitement.
(Avec agences)
Vous avez un projet immobilier en vue ? Yakeey & Médias24 vous aident à le concrétiser!




